Kjemiske metoder for vannmykning. vannmykner
Kroppen vår mottar opptil 25 % av mineralene fra vann. Dermed påvirker vannkvaliteten direkte helsetilstanden vår. Tross alt, gjennom det, skjer prosessen med assimilering av produkter, inkludert skadelige stoffer, veldig raskt. Og derfor, for å unngå problemer, bør vannmykning utføres. I denne artikkelen vil vi vurdere spørsmålet om for høyt innhold av hardhetssalter i vann.
Fra denne artikkelen vil du lære:
Hvorfor må vann mykgjøres?
Hva er metodene for vannmykning
Hvilke filtre kan gjøre vannet mykere
Hvor bra er et omvendt osmosesystem?
Hvorfor vannmykning for hjemmet er et presserende problem
Hva er vannhardhet? Dette konseptet betyr hvor mye jordalkalimetallsalter det inneholder. I Russland er det egne kriterier for å bestemme hardheten til drikkevann, som er etablert av GOSTs og sanitære og epidemiologiske regler og forskrifter. For eksempel SanPiN 2.1.4.1974-01. Andre land har sine egne standarder. For eksempel, i USA er dette standardene til byrået som beskytter miljø. I EU, rådsdirektiv 98/83/EC.
Offisielt måles indikatoren for vannhardhet i grader, og en grad er lik 1 meq / l, i henhold til GOST 31865-2012. Den tillatte terskelen bør ikke være høyere enn 7 mg-eq/l.
Vannhardhet er klassifisert som følger:
mindre enn 1,5 mg-eq / l - veldig mykt vann;
fra 1,5 til 4 mg-eq/l - mykt vann;
fra 4 til 8 mg-eq / l - vann med middels hardhet;
fra 8 til 12 mg-eq/l - hardt vann;
over 12 mg-eq / l - veldig hardt vann.
Dette er standarder for drikkevann som brukes til økonomiske og husholdningsformål. For utstyr, for eksempel dampkjeler, pålegges det enda strengere standarder. Og dette er ikke overraskende, fordi kjelen må fungere ordentlig, og hardt vann kan føre til sammenbrudd. Og derfor er indikatorene for begrensningen halvparten av verdiene gitt i SanPiN.

Hvorfor er dette vannet farlig? Bruken fører til funksjonsfeil i mage-tarmkanalen og problemer forbundet med gastrisk motilitet. Salter samler seg gradvis i kroppen, leddsmerter oppstår, og det dannes steiner i galleblæren og nyrene. I tillegg avsettes disse stoffene på huden og håret. Saltavleiringer forblir på utstyret, samme vannkoker, vaskemaskin, rørleggerarbeid... Dette vannet er også skadelig for lin. Det ødelegger rørledninger. Hva annet? Siden saltavleiringer på deler og komponenter av utstyr fører til et fall i varmeoverføringskoeffisienten, øker også drivstofforbruket. Derfor anbefales avmykning av vann til hjem og produksjon på det sterkeste dersom det ikke oppfyller standardene.
Fra brønner og brønner kommer vann hardt, siden i jordens tarmer er alt uten unntak, og i dette tilfellet er det nødvendig med mykning.
Hvordan forstå at vann må mykes opp? Dette er indikert med en rekke tegn:
Etter vask er tøyet hardt, hvite flekker observeres på det.
Det kreves mer vaskemiddel enn anbefalt av produsenten, og det skummer ikke godt nok.
Veggene i vannkokeren er dekket med skala.
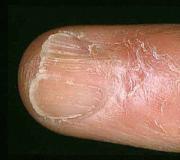
Etter hygieneprosedyrer virker huden tørr og stram.
Kraner er belagt.
Før du myker opp vann til hjemmet ditt, finn ut sammensetningen av vannet som kommer fra vannforsyningen. Utfør en kjemisk analyse. Anbefalinger: hvis du bor i et landlig hus (hytte eller privat bolig), velg en automatisk installasjon for kontinuerlig vannmykning.
Derfor bør myknet vann brukes for å forhindre helseproblemer og forlenge levetiden til husholdningsutstyr. Automatiske innstillinger, som kontinuerlig myker opp vann, er best egnet for bruk i hytter og landsteder. Riktig valg systemet er bare mulig etter å ha bestemt sammensetningen av vann, i denne forbindelse er det umulig å gjøre uten dens kjemiske analyse.
Hvordan er det mulig å myke opp vannet til huset
Eksistere ulike metoder vannmykning: kjemisk, mekanisk og fysisk. Så, kjemisk rengjøring utføres ved hjelp av reagenser, mekanisk er bruk av fysiske barrierer, og fysisk innebærer at naturkreftene brukes, for eksempel magnetisme. Disse metodene kombineres for å oppnå det beste resultatet.
Hva er formålet og betingelsene - en slik rensemetode er også valgt. Dette bestemmes av nivået på vannhardhet, av hvor stor eller liten husbygningen er. Deretter bør du vurdere de vanlige metodene for å myke vann for hjemmet.
Kjemisk rengjøring. Det brukes spesielle reagenser, som kalles koagulanter. Som et resultat av interaksjonen mellom kalsium og magnesium dannes en uløselig forbindelse, som gradvis legger seg på filterveggene. Kalk, natriumhydroksid, sodavann, fosfonater brukes som reagenser. Denne metoden er kun egnet for behandling av teknisk vann, for eksempel i et kjelerom.
Rensing av polyfosfat. Denne enkle og rimelige reagensrengjøringsmetoden mykner prosessvann. Hardhetssaltet og natriumpolyfosfatet reagerer, hvoretter det dannes en uløselig film, bestående av kalsium- og magnesiumpolyfosfat, og samtidig mettes vann med natriumioner.
Ionebyttemykning. Dette er en rimelig og effektiv teknologi: vann passerer gjennom et mykgjørende filter fylt med ionebytterharpiks. Etter å ha passert gjennom sistnevnte, som et resultat av ionebytterreaksjonen, dannes en harpiks fra kalsium- og magnesiumioner av vann, og prosessen med å berike den filtrerte væsken med natriumioner, som er trygge for menneskers helse og utstyr, er også startet.
Fordelene med denne teknologien inkluderer det faktum at ionebytterharpiksen har evnen til å regenerere, det vil si at den kan gjenopprettes. For å gjøre dette er det nok å vaske harpiksen, som vanlig bordsalt brukes til. Mange vannmyknere er utstyrt med multiprosessorkontroll, som gir den nødvendige automatiske aktiveringen av regenereringsmodusen.
Vannbehandling ved denne metoden fører ikke til nedbør, det vil si at det ikke er nødvendig å kjøpe ekstra filtre. Denne typen filter er egnet til å myke opp drikkevann og industrivann.
Filtrering basert på prinsippet om omvendt osmose. Ved bruk av denne teknologien brukes en membran laget av aromatisk polyamid eller celluloseacetat for å myke opp vann. En membran av denne typen garanterer nesten fullstendig demineralisering, og selvfølgelig reduseres stivhetsindeksen. Som et resultat mottar forbrukeren vann nær destillat.
Denne rengjøringsmetoden har følgende fordeler: installasjonen har små dimensjoner og lavt energiforbruk. Ulempen er at filtrene er dyre, membranen må av og til skiftes, og det brukes mye penger på dette.
Omvendt osmosesystemet fungerer under den obligatoriske betingelsen at et grovt forfilter og et kunstig mineraliseringsetterfilter er installert. Ved hjelp av sistnevnte blir vann beriket med kalsiumsalter (fra 40 mg/l), magnesium (fra 20 mg/l), fluor, kalium og andre kjemiske elementer opptil 100 mg/l.
Bruk av en mineralisator er nødvendig, siden omvendt osmosesystemet renser vannet så mye at det dannes en kjemisk ren forbindelse. Hvis du drikker destillert vann i lang tid, vaskes makro- og mikroelementene den trenger ut av kroppen.
Magnetisk filtrering. Implementeringen av magnetiske og elektromagnetiske metoder har funnet sin anvendelse i enheter liten størrelse, som er installert på rørledningens indre vegger. Vann føres gjennom denne typen filter, med et magnetfelt som virker på magnesium- og kalsiumsaltene, og får dem til å danne en uløselig form. Fjerning av sediment fra vannforsyningssystemet utføres på grunn av vannstrømmen.
Et lignende filtreringssystem brukes hvis skala er din fiende, og det er nødvendig å beskytte kjeler, søyler og varmtvannsberedere, vaskemaskiner eller oppvaskmaskiner som er installert i privateide hus og hytter fra det.
Utbredt bruk av beboere landsteder kombinert metode. For eksempel brukes et magnetisk filter i teknisk vannforsyning, et omvendt osmosesystem brukes for å dekke drikkebehov (en mineralisator er absolutt nødvendig). Bruken av det siste alternativet innebærer at dette ikke er en billig fornøyelse, så installer et ionebytterfilter for å optimalisere kostnadene. Det utmerker seg ved sin allsidighet, høye ytelse, og vannet som mykgjøres av det kan like vellykket brukes til mat og brukes i husholdningsutstyr.
Filtre som garanterer mykning av vann i huset
Etter å ha bestemt den optimale teknologien, er det viktig for kjøperen å ikke gjøre feil når han velger en konstruktiv løsning.
Kompakt filter. Dette filteret er festet på røret gjennom hvilket vann kommer inn i enheten, for eksempel i en vaskemaskin eller kjele. Det er også mulig å bruke et delvis løselig reagens - natriumpolyfosfat, helles inni, eller bruk av en kunstig opprettet magnetfelt. Dette filteret er praktisk, men det er designet for å myke opp vann, som etter rengjøring kun har et husholdningsformål eller kun tjener ett utstyr.
hovedfilter. Systemet mottar vann fra et rør som dette filteret er montert på. Dette sikrer at alle mulige problemer forbundet med mykgjøring av vann, men prisen på filteret er høy, og prosessen med driften er ganske treg.
patronfilter. Vanligvis er hvert filter av denne typen utstyrt med en gjennomsiktig kolbe med en utskiftbar ionebytterharpikspatron installert i sistnevnte. Standardstørrelsesfilteret (ti tommer) er designet for fire tusen liter eller non-stop drift i en periode på seks måneder. Deretter byttes patronen. Dette systemet har en ganske lav arbeidsressurs og det er ingen mulighet for gjenoppretting.
Skaptype filter. Disse små installasjonene finner sin anvendelse i kontorer og leiligheter. Denne typen system implementerer ionebytterteknologi. Dette filteret har 50 % lavere absorpsjonsmiddelforbruk enn andre typer myknere, og fungerer derfor mer økonomisk. Det behandlede vannet kan trygt drikkes, fungerende husholdningsapparater vann gjør absolutt ingen skade. Filteret har en nyanse: det takler bare små volumer og er ikke egnet for et hus med et stort område. Det beste alternativet– Dette er en hytte der det bor fem-seks leietakere.
Ionebytterfilter. Enheten er en kolonne med salttanker. Hver vertikal enhet er en tank med en ionebytterharpiks inni. Vannet som passerer gjennom dem er gjenstand for mykning. Det er tenkt at systemet kan utstyres med en saltbeholder, som brukes i regenereringsprosessen. Etter at den er nådd kritisk grense, endres filtreringsmodusen til regenerering og saltvannet ledes gjennom tanken. Dyre systemer har to filtreringskretser. En krets er involvert i regenereringsprosessen, mens den andre opererer med full kapasitet.
Vannmykningssett i vår katalog
For en gjennomsnittlig familie som bor i et privat hus, er et vannmykningsfilter egnet, med en kapasitet på opptil halvannen kubikkmeter i timen. Uten erstatninger som oppstår av nødvendighet, er fyllstoffet i stand til å tjene opptil ti år.
Vannmykning ved omvendt osmose
Nylig har omvendt osmosefiltre blitt ansett som den beste løsningen hvis du trenger å rense eller myke opp vann til hjemmet ditt. Men denne enheten har mange ulemper, noe som tyder på at det er uhensiktsmessig å investere i en slik mykner.
Oppløste hardhetssalter kan ikke fjernes med nettingfiltre. Men et filter av membrantypen kan takle denne oppgaven.
Det omvendte osmosesystemet har lav produktivitet, som anses som dens største ulempe. Dette kompenseres av at det er installert flere kretser som fungerer parallelt. Hver av dem har en separat membran (et sett med nødvendige filtre), samt en pumpe som injiserer økt trykk for effektiv funksjon av denne enheten.
For å installere denne typen filter, må du finne nok plass, samt å isolere dette rommet slik at støy ikke kan høres i andre rom, og løse andre relaterte problemer.
Men praksis viser at disse kraftige installasjonene svært sjelden brukes i hverdagen. Deres funksjonalitet er bredere enn for en enkel vannmykner for et privat hus, men samtidig er slikt utstyr for dyrt, og dets videre drift er langt fra den billigste. Installasjon av disse systemene utføres i fabrikker hvor for dyp rengjøring arbeidsvæsker, må den teknologiske prosessen følges strengt.
Installasjonen av omvendt osmose har noen flere begrensninger som de som planlegger å kjøpe dette systemet bør være klar over:
hver 4-6 måned - mekaniske forfiltre;
hver 3-4 måned - filtre fylt med aktivt kull (også foreløpig);
hver 8.-12. måned - etterfiltre med fyllstoffer med aktivt kull);
hvert annet eller annet og et halvt år - en omvendt osmosemembran.
Uten god forfiltrering av mekaniske urenheter oppstår det svært rask forurensning av patronene. Risikoen er spesielt høy hvis gammel by nettverksteknikk eller en personlig brønn ble boret "på sanden" (grunn dybde).
Hver utstyrsmodell oppfyller klare krav til hvordan sammensetningen av utløpsvannet skal være, og disse standardene er satt av produsentene av disse systemene.
I tillegg er det nødvendig å observere området for opprettholdt temperatur og vann, som er satt av produsenten. I de fleste tilfeller vil det være nødvendig å installere restriktive ventiler ved innløpet og også å bruke pumper med automatisk styring av og på.
For at utstyret skal fungere av høy kvalitet, er det nødvendig å endre individuelle elementer i tide:
Av kjemisk oppbygning vann renset ved omvendt osmose tilsvarer destillert væske. Det er generelt akseptert at det kan skade helsen til en viss grad, siden hvis en person drikker dette vannet hver dag, vil han ikke motta mineralene som er nødvendige for kroppen hans. I tillegg liker noen eiere ikke å drikke så høyt renset vann.
Av denne grunn er spesielle blokker - mineralisatorer - noen ganger koblet til omvendt osmoseanlegg som et tillegg. Med deres hjelp kommer kalsium og magnesium inn i vannet, det vil si at væsken er mettet med disse elementene. Systemet kan utstyres med en ventil som skal sørge for at en slik enhet inngår i den generelle kretsen i de tilfeller et slikt behov oppstår.
Alt som ble skrevet ovenfor fører til behovet for å vurdere i detalj muligheten for å kjøpe et omvendt osmosefilter for å bruke det til å myke opp vann til hjemmet.
Biokit tilbyr bredt utvalg omvendt osmosesystemer, vannfiltre og annet utstyr som er i stand til å returnere springvannet til dets naturlige egenskaper.
Våre spesialister står klare til å hjelpe deg:
koble til filtreringssystemet selv;
forstå prosessen med å velge vannfiltre;
velg erstatningsmaterialer;
feilsøke eller løse problemer med involvering av spesialistinstallatører;
finne svar på spørsmålene dine over telefon.
Betro vannrensesystemer fra Biokit - la familien din være sunn!
Hvordan myke opp hardt vann. Måter, tips, skader og fordeler, forskjellige metoder, funksjoner og akseptable indikatorer.
Vi har alle hørt om farene ved hardt vann - ikke bare for kjøkkenmaskiner og varmeutstyr, men også for menneskekroppen. Imidlertid vet få mennesker at dens stivhet er forskjellig i "opprinnelse", og dessuten er det ikke et absolutt onde. Derfor skal vi i dag se på hvordan du kan gjøre den mest effektive mykningen av vann til drikke og husholdningsbehov for å få mest mulig ut av det.
Funksjoner av hardt vann
Vann blir hardt av oppløste salter - kalsium- og / eller magnesiumforbindelser (kationene til sistnevnte er mye mindre vanlige). Det er andre elementer, hvis tilstedeværelse kan påvirke de endelige indikatorene for stivhet, for eksempel mangan, strontium, barium. Men deres innflytelse er så ubetydelig at den rett og slett ikke blir tatt i betraktning.
Den generelle hardhetsindeksen er vanligvis delt i samsvar med sammensetningen av saltene:
- Karbonat eller midlertidig hardhet - bestemmer innholdet av Ca- og Mg-bikarbonater i vann ved et pH-nivå som overstiger 8,3 enheter. Det kan enkelt håndteres ved langvarig koking - etter en time vil saltene ganske enkelt gå i oppløsning under påvirkning av høy temperatur og utfelles.
- Ikke-karbonat hardhet kalles konstant, fordi det ikke er så lett å bli kvitt det. Det bestemmes av innholdet av stabile salter av forskjellige syrer, som ikke brytes ned og må fjernes med andre metoder, for eksempel omvendt osmose.
I sum gir disse to indikatorene bare den generelle stivheten, selv om det er vanskelig og dyrt å beregne dem separat. Vanligvis brukes spesielle reagenser eller indikatorstrimler for å bestemme det faktiske saltinnholdet.
Men du kan finne ut at systemet ditt har hardt vann uten laboratorietester. I bruksprosessen gir den mange problemer som rett og slett er umulig å ignorere:
- Hvite merker på vaskede klær;
- Svak skumdannelse vaskemidler, og som en konsekvens - deres ineffektivitet;
- Skala på veggene til vannkokeren (og forestill deg hva som skjer med varmeelementene til kjeler, vaskemaskiner og oppvaskmaskiner);
- Stadig dukker plakett på blandebatteriet og vasken.

Hardt vann forårsaker også betydelig skade på menneskekroppen. Følelsen av tørr hud etter kontakt med et slikt miljø er ikke annet enn å vaske av den beskyttende lipidfilmen fra overflaten. Og bruken av dette vannet inne uten foreløpig mykning kan provosere urolithiasis.
Men dette betyr ikke at vannmykning skal være total, selv om det brukes til drikking og matlaging. En væske fullstendig blottet for salter fører til en mangel på kalsium- og magnesiumioner i kroppen, noe som negativt påvirker funksjonen til det kardiovaskulære systemet. Skaden og fordelene ved hardhet i drikkevann er et av de medisinske paradoksene. Men det er tillatt ganske enkelt - overholdelse av tiltaket.
Fra legenes synspunkt er bruken av for hardt, så vel som for mykt vann, uakseptabelt. Her må du holde deg til den gylne middelvei.
«Remyknet» vann kan skade både stålrør og vannrør. varmesystemer– på grunn av det er de mer utsatt for korrosiv slitasje og har kortere levetid enn rørledninger som transporterer harde medier.
Folkemåter for mykning
Våre bestemødre møtte også problemene med hardt vann, og de gjettet i det minste om farene ved å bruke det. Derfor er det nok enkle og rimelige måter å myke opp i folkevisdommens sparegris. Vi presenterer de mest populære av dem.

Koking (og ikke i en vannkoker, men på en komfyr, siden den ønskede effekten av nedbrytning av hardhetssalter bare kan oppnås med langvarig oppvarming). Etter dette skal væsken få sette seg i et døgn, og først da skal den dreneres forsiktig uten å røre opp sedimentet i bunnen.
Frysing er en mer skånsom måte som lar deg i det minste delvis bevare nyttige stoffer i vann og ikke ødelegge smaken. En gjennomsiktig beholder med vann må sendes til fryseren og overvåke frysingen. Så snart 75-80% av det totale volumet blir til is, tas karet ut og væskeresten dreneres - salter konsentreres i det, noe som gir høy stivhet.
Bosetting. Du trenger bare å helle vann i en beholder og sette den vekk fra solstråler i 3-6 dager. Etter det må du drenere de øvre lagene forsiktig uten å forstyrre sedimentet. Slikt vann er ikke egnet til å drikke, men det er ganske egnet for husholdningsbruk.
Tilsetning av silisium eller shungitt - mineraler som bokstavelig talt absorberer hardhetssalter. Våre oldefedre foret brønner med flint for å myke opp vannet som er lagret i dem. En enklere måte er tilgjengelig for oss: du trenger bare å senke de sterile steinene av silisium eller shungitt ned i en beholder med drikkevann. Naturlige absorbenter vil absorbere salter i løpet av 2-3 dager, selv om mange anbefaler å øke denne perioden til en uke.
Forsåpning er en av måtene å forberede vann til vask. Det vil være nødvendig å rive 15-20 g husholdning eller toalettsåpe og fortynn den i 0,5 l vann til den er helt oppløst og skum vises. Denne mengden er nok til en bøtte med væske, hvoretter du må stå alt i minst en natt - såpen vil reagere med saltene og sende dem til sediment. Om morgenen helles løsningen forsiktig i en annen beholder og legges til den. borsyre(2-3 ss).

Moderne metoder
For oss, moderne mennesker, finnes det enklere måter å myke opp hardt vann. For å gjøre dette er det nok å kjøpe og sette inn mykningsfiltre med ionebytterharpiks i forsyningssystemet. De er doble tanker og fungerer etter følgende prinsipp:
- Hardt vann kommer inn i rommet med harpiks, som "ekstraherer" kalsium, magnesium og andre jordalkalielementer fra det.
- Den utarmete væsken strømmer inn i den andre tanken med vanlig bordsalt, hvor den er beriket med natriumioner - mye mer nyttig for kroppen.
- Rester med "skadelige" elementer fjernes sammen med avløp.
Som et resultat får vi trygt og velsmakende myknet vann med normalisert hardhet. Den kan brukes både til husholdningsbehov og til drikking eller matlaging.
Ulike land har sine egne hardhetsstandarder. Våre maksimale indikatorer for drikkevann er satt til 7 mg-eq/l, for teknisk vann - ikke mer enn 9 mg-eq/l.

Den mykgjørende effekten oppnås også etter rennende vann gjennom et omvendt osmosesystem. Den fungerer på en helt annen måte: den tvinger væsken gjennom en spesiell membran med svært små porer (0,0001 mikron i størrelse) og fanger urenheter på molekylnivå. Dermed frigjøres vann ikke bare fra salter, men også fra bakterier og andre fremmedelementer, og blir praktisk talt til et destillat.
Akk, konstant bruk av det i mat gjør mer skade enn nytte. Derfor, etter rengjøring og mykgjøring, er det ønskelig å føre slikt vann gjennom et system med mineralisatorer, som vil berike det med trygge stoffer og gjenopprette optimal hardhet. Imidlertid er det ganske egnet for husholdningsbehov.
For å beskytte utstyr mot hardt vann, brukes forskjellige tilsetningsstoffer:
- Mat, brus;
- sitronsyre;
- Eddik;
- Enhver vannmykner basert på polyfosfater (Calgon, Eonite, Sodasan, etc.).
Hvorfor er vannmykning så nødvendig?
Når du bodde i en leilighet eller et landsted og brukte vann fra en byvannforsyning, en brønn, en brønn eller en annen kilde til vanninntak, måtte du håndtere de ubehagelige konsekvensene av å bruke hardt vann. Tørr hud etter en dusj, stivhet i klær og tekstiler etter vask, dårlig skumdannelse av såper og vaskemidler, samt hvite avleiringer på rørleggerutstyr og utseende av kalk under koking - alt dette er de mest synlige tegnene på en overdreven konsentrasjon av hardhet salter i vann. Det er umulig å ikke merke seg de skadelige konsekvensene av påvirkningen av hardt vann på menneskekroppen: problemer med det kardiovaskulære systemet, nedsatt motilitet i magen, leddsykdom og uønskede avleiringer i nyrene eller galleveiene. I tillegg til alt det ovennevnte, dannes kalk under drift av vannoppvarmingsutstyr (kjeler, kjeler, vaskemaskiner, oppvaskmaskiner, etc.), bidrar til at de feiler for tidlig.
Det er også uakseptabelt å bruke vann med høy saltholdighet i industrien, noe som forårsaker brudd på teknologiske og kjemiske prosesser i produksjon av mat, drikke, forbruksvarer, etc. Behovet for å eliminere vannhardhet spiller også en viktig rolle i energisektoren, hvor dannelsen av kalk forstyrrer ytelsen til kostbart varmevekslerutstyr og varmesystemer, samtidig som det reduserer varmevekslingsegenskapene deres kraftig (som senere øker drivstoffkostnadene), og forårsaker fullstendig feil.
Konseptet med hardt vann. Hva forårsaker vannhardhet?
Vannhardhet karakteriserer konsentrasjonen (tilstedeværelsen) i den av kalsiumioner (Ca 2+), magnesium (Mg 2+), strontium (Sr 2+), barium (Ba 2+), jern (Fe 2+) og mangan (Mn) 2+). Men tilstedeværelsen i naturlig vannøks direkte av kalsium- og magnesiumioner er mye høyere enn den totale tilstedeværelsen av andre listede ioner. Av denne grunn refererer vannhardhet til den totale mengden kalsium- og magnesiumioner. Hardhet er forskjellig i midlertidig (karbonat), avleiringsdannende, forårsaket av tilstedeværelsen av kalsium- og magnesiumbikarbonater, så vel som permanent (ikke-karbonat), ofte på grunn av tilstedeværelsen av sulfater og klorider og ikke frigjort under koking.
I dag, angående hardheten til vann, er det en rekke krav og normative dokumenter satt sammen av ulike avdelinger og orientert mot ulike typer forbrukere. Standarder for totalt saltinnhold, uavhengig av overflate el grunnvann, for systemer for husholdnings- og drikke- og husholdningssystemer, kommer i større grad ned til kravene til SanPiN "Drikkevann", der MPC (maksimal tillatt konsentrasjon) av hardhetssalter ikke bør overstige mer enn 7 mg / l. Men samtidig bør det rettes behørig oppmerksomhet til vannkvalitetsstandarder for varmtvannsforsyning, varmeforsyning, damp- og varmtvannskjeler, der driftsreglene for enheter krever MPC-hardhet betydelig lavere enn SanPiN-standarder (mindre enn 2 mg / l). Det bør også bemerkes at konsentrasjonen av kalsium- og magnesiumioner er relativt lavere, etablert i kvalitetsstandardene til EU, Verdens helseorganisasjon og amerikanske nasjonale standarder, som ikke overstiger 5 mg/l. Vesentlig ulike krav til saltholdighet i vann og systemer industriell bruk(noen ganger til fullstendig fravær), der de nødvendige konsentrasjonene regulerer de tekniske og kjemiske prosessene i produksjonen. Oppmerksomhet på MPC for vannhardhetssalter i kraftindustrien er rettferdiggjort av den teknologiske og økonomiske effektiviteten til utstyret (mindre enn 1 mg / l), og er mer rettet mot å forhindre hovedproblemet - skaladannelse.
Vannmykningsmetoder
1. Vannmykning ved ionebytte den mest populære og mye brukte metoden for å myke opp vann fra en brønn eller vannforsyning i drikke- og husholdningssystemer. Denne metoden består i evnen til ionebyttermaterialer (harpikser) til å bytte ioner av hardhetssalter (kalsium, magnesium, etc.) med ioner av andre molekyler som ikke forårsaker beleggdannelse. Også denne metoden, avhengig av typen harpiks som brukes, lar deg trekke ut jernforbindelser og om nødvendig redusere mineraliseringen av vann. Således sikrer vannmykning ved ionebytting, i motsetning til andre metoder (unntatt omvendt osmose), eliminering av vannets hardhet, og konverterer dem ikke (uten å fjerne dem) til en form som ikke forårsaker kalk.
For husholdnings- og drikkeformål, for å myke opp vann fra en brønn, brønn eller vannforsyning, brukes ofte filtre med matkvalitets kationbytterharpiks i Na-form. Disse harpiksene er designet for å eliminere vannhardhet ved å fjerne kalsium- og magnesiumioner, bytte dem ut med natriumioner (uten å øke mineraliseringen av vann betydelig). Disse filtrene inkluderer:
- Vannmyknere i WS-serien (Lewatit S1567) . Automatiske og mekaniske filtre for eliminering av vannhardhet med tyskprodusert filtermateriale Lewatit S 1567.
- Kabinettvannmyknere: North Star, BWT, Atoll Excellece L, Atoll Excellece R. Kompakte automatiske vannhardhetsfiltre av amerikansk og europeisk produksjon.
- Installasjon av mykning av kontinuerlig handling WS TWIN (Lewatit S1567) . Automatiske vannherdende filtre for kontinuerlig mykgjøring av vann uten regenerering. Filterbelastning - Lewatit S 1567.
For å bruke kationbytterfiltre under forhold med høy konsentrasjon av jern, mangan, hydrogensulfid eller organiske forbindelser i vann, er deres foreløpig fjerning nødvendig. Av denne grunn, i komplekser av vannbehandlingssystemer, installeres de etter foreløpig grovrengjøring, doseringssystemer, vannlufting, vannstrykestasjoner, etc., avhengig av teknologiene som brukes.
Ellers, for engangseliminering av hardheten til vann, jern, mangan eller deres organiske forbindelser, uten bruk av foreløpige "oksidasjonsmidler" (dosering eller lufting) og jernfjernere, brukes kombinerte harpikser bestående av en blanding av kation -utveksling, anionbytter og inerte materialer. Disse filtrene inkluderer:
- filtre for vannmykning og fjerning av jern Geyser Aquachief (Ekotar B) eller stasjoner for vannfjerning og mykgjøring ECO A (Ecomix A) . Automatiske og mekaniske filtre for eliminering av vannhardhet, oppløst jern og mangan med separat salttank. Filtermaterialer Eocar B og Ecosoft Mix A.
- skapvannmyknere ATOLL-serien: EcoLife SM , Excellece LM . Amerikanskproduserte automatiske filtre for eliminering av vannhardhet, oppløst jern og mangan i ett komposittfilterhus sammen med en salttank.
- vannmykningsanlegg ECO (Ekomiks C) . Automatiske og mekaniske filtre for å eliminere vannhardhet, oppløst jern, mangan med økt konsentrasjon av organiske forbindelser (overskredet permanganatoksidasjon) med separat salttank.
Både for industri, energi, husholdning (spesielt damp- og varmtvannskjeler), og husholdnings- og drikkeanlegg (inkludert varmt og kaldt vann for landsteder), er generell mineralisering ikke mindre viktig sammen med vannhardhet. Med økt mineralisering, mykgjøring av vann Ionebyttemetoden lar deg også effektivt redusere innholdet av mineralsalter. Vannmineralisering er imidlertid noe mer kompleks enn å myke opp. Denne prosessen er basert på bruk av anionbytteregenskaper til harpikser etter foreløpig kationisering. For å gjøre dette, i vannbehandling, er det forskjellige ett- og flere-trinns ordninger for kationisering og anionisering.
De mest populære merkene av ionebytterharpikser er: Lewatit, Ecosoft Mix, Dowex, Purolite, Ecotar, PURESIN, etc. Det er verdt å merke seg det eksisterende utvalget av harpikser av samme merke, som er forskjellige i egenskaper, sammensetning, egenskaper og formål med deres anvendelse. Av denne grunn anbefaler vi at du rådfører deg med en spesialist før du velger og kjøper nødvendig mykner eller skifter tilbakefylling i et eksisterende filter.
2. Vannmykningsmetode ved bruk av omvendt osmose innebærer bruk av semipermeable membraner laget av celluloseacetat eller aromatisk polyamid. Beholder nesten alle ioner denne metoden mykgjøring gir den dypeste mulige demineralisering og eliminering av hardhetssalter. Rensegraden av omvendt osmosesystemer er opptil 99 %. Sammenlignet med ionebytterfiltre er deres design mindre samlet og representerer metallskrott med membraner (hvis antall og størrelse avhenger av nødvendig kapasitet til vannbehandlingsanlegget), boosterpumpe, systemenhet, doseringspumpe, små komponenter osv. Når det rensede vannet treffer membranen, går en del av det som er filtrert nesten til destillat, til forbrukeren, og resten med alle urenheter går inn i dreneringssystemet, eller går tilbake til filtrering.
I tillegg til liten størrelse og enkel design (relativt vannmykner ionebyttemetode) av omvendt osmosesystemer, er det også verdt å merke seg slike fordeler som: lavt energiforbruk, relativt lite driftskostnader og mulighet for å slippe kraftfôret ut i kloakken. Men med alt dette er det verdt å vurdere behovet for forbehandling av det behandlede vannet for en lang levetid for membranene. Den tillatte konsentrasjonen av urenheter i det behandlede vannet reguleres av membranenes driftsegenskaper. Det er også nødvendig å ta hensyn til det høye vannforbruket (mens du bare mottar 20-25% rent, resten tappes), høye kostnader på kjøpstidspunktet og anbefalt kontinuerlig drift.
Til dags dato, metoden vannmykner Ved hjelp av omvendt osmose er en av de mest lovende metodene for å fjerne vannhardhet og rense det generelt. Vannmykning med omvendt osmose er mye brukt i tapping av drikkevann, produksjon av alkoholholdige og alkoholfrie drikkevarer, i næringsmiddelindustrien, i hytter, landsteder, leiligheter osv. Blant våre produkter finner du omvendt osmosesystemer fra produsenter som: Atoll, Aquapro, Geyser, Osmosis RO, etc.
3. Reagensvannmykningsmetode er en behandling (ved dosering) av renset vann med ulike reagenser og koagulanter som binder kalsium og magnesium til dårlig løselige forbindelser, som sammen med andre suspenderte urenheter i ettertid holdes tilbake i ulike sedimentasjonstanker eller klaringsfiltre. I dette tilfellet brukes kalk, soda, natriumhydroksid, syrer, fosfonater etc. Som reagenser brukes ofte reagensmetoden med vannmykning for å myke opp, eller med andre ord, "stabilisere" varmeenergisystemene til industrianlegg, boliger og fellestjenester, fyrhus sentralvarmeanlegg mv.
Hovedformålet med reagensbehandlingen er å forhindre avleiring, korrosjon og mikrobiologisk begroing av varmevekslerutstyr, inkludert rørledninger, ved lave og høye temperaturer. Det er mye brukt i overflatevannsbehandling, hvor det er stor sannsynlighet for et høyt innhold av farlige stoffskifteprodukter fra levende organismer, alger, bakterier og andre mineralske eller organiske forurensninger. For dypere vannmykning kan den brukes i vannbehandlingssystemer sammen med påfølgende kationbytterfiltre.
I motsetning til lukkede varmeforsyningssystemer (varme) brukes reagensmetoden for vannmykning i åpne systemer praktisk talt ikke, siden kravene til kvaliteten på nettverksvann i åpne systemer må oppfylle kravene til "drikkevannskvalitet".
4. Magnetisk og elektromagnetisk metode for vannmykning brukes for å forhindre dannelse av belegg i termiske systemer, dampgeneratorer, kaldt- og varmtvannsforsyningssystemer i industri, landsteder, hytter, leiligheter osv., og er en prosess for å føre vannstrøm i en rørledning gjennom et magnetfelt. Under påvirkning av et magnetisk felt krystalliserer kalkdannende urenheter av karbonathardhet (kalsium, magnesium og jern) til en uløselig og ikke-dannende fast belegg på veggene til rør eller varmtvannsberedere, en løs form, mens de blir værende i vannet kolonne. Samtidig ødelegges også tidligere dannede avleiringer over tid, og sammen med vannstrømmen fjernes de lett fra rørsystemet.
For å skape disse magnetfeltene i rørledningen i vannbehandling, brukes spesielle enheter med permanente magneter eller elektromagneter. I motsetning til vannmykner ved ionebytte- og omvendt osmosesystemer er magnetiske myknere de mest kompakte, enkle å installere, betjene og økonomiske. Installasjoner med elektromagnetisk påvirkning består av en elektronisk enhet som sender signaler til en isolert ledning viklet rundt et vannrør. Takket være signalene som kommer med den spesifiserte renheten, avgir disse ledningene et elektromagnetisk felt som går gjennom som det rensede vannet mykes opp.
For noen vil uttrykket "hardt vann" virke som en litterær oksymoron, men det er mange mennesker som er kjent med denne kvaliteten på vann. Hvordan bestemme graden av hardhet og hvorfor myke opp vann - vi vil fortelle i denne artikkelen.
Hardt vann er årsaken til dannelsen av saltavleiringer, nyrestein, hjerte- og karsykdommer. 80% av sykdommene drikker en person med vann. 90 % av feil på varmtvannsberedere og annet utstyr som arbeider med vann er forårsaket av høy alvorlighetsgrad.
Hva er hensikten med vannmykningsprosessen?
Vannhardhet er en kombinasjon av dets fysiske og kjemiske egenskaper assosiert med innholdet av oppløste salter av jordalkalimetaller. Først av alt er kalsium og magnesium hardhetssalter. I det naturlige miljøet regulerer de ulike kjemiske prosesser. Vannets hardhet påvirkes hovedsakelig av avsetningen. Elver og innsjøer fylles på fra underjordiske kilder som renner i kalksteinslag og beriker vannet som passerer gjennom dem med hardhetssalter. Overflatevann inneholder betydelig mindre kalsium og magnesium enn dypt vann. Vannets hardhet i naturlige kilder når sitt maksimum om vinteren, og sitt minimum om våren, takket være snøsmelting.
Det er tre typer vannhardhet:
- Generell. Dette er den totale konsentrasjonen av magnesium- og kalsiumioner.
- Karbonat. Dets andre navn er midlertidig, siden indikatorene avhenger av innholdet av kalsium- og magnesiumkarbonater og bikarbonater i vann, som nesten fullstendig elimineres ved koking.
- Ikke-karbonat, tvert imot, er en konstant verdi, fordi det skyldes tilstedeværelsen av magnesium- og kalsiumsalter, som ikke påvirkes av temperaturendringer.
I SI-systemet måles vannhardhet i mol pr kubikkmeter -mol/m³, men milligramekvivalenter per liter brukes også i praksis -mg-ekv/l. I henhold til normene til SanPiN bør hardheten til drikkevann ikke være mer enn 7 mg-eq / l. Nødvendig vannhardhet for ølproduksjon -opptil 4 mg-eq/l, brus -0,7 mg-ekv/l.
For hardt vann er en av årsakene til dannelsen av nyrestein, siden kalsium- og magnesiumbikarbonater gjør det vanskelig for mage og tarm å fungere. De såkalte saltavleiringene i leddene kan også være et resultat av å drikke hardt vann. Hardhetssaltene i den samhandler aktivt med såper, sjampoer, balsamer og andre lignende produkter, danner et bunnfall og reduserer effektiviteten. På grunn av ødeleggelsen av den naturlige fettbeskyttelsen, er porene på menneskets hud tilstoppet med neoplasmer, noe som gjør det vanskelig å puste. Dette kan føre til tørrhet, akne, flass, samt brudd og hårtap. Hardt vann påvirker også matlagingen på en dårlig måte, og ødelegger de gunstige stoffene i ingrediensene.
Hardt vann reduserer levetiden til husholdningsapparater betydelig: oppvaskmaskiner, kjeler, vannkoker, etc. På grunn av krystalliseringen av salt dannes det avleiring, som deretter fører til korrosjon og brudd. Som i tilfellet med sjampo, når du vasker i hardt vann, er en del av "kreftene" til pulveret rettet mot å nøytralisere effekten, men her, i tillegg til det banale overforbruket av vaskemidler, er sjansene for å få lin med flekker eller flekker. øke. De oppstår også på grunn av kalkdannelse på "innsiden" av vaskemaskinen.
I urbane områder er hardt vann nå nesten aldri funnet, men i privat sektor og landsbygda situasjonen er annerledes. Vanligvis bruker innbyggerne deres vann fra en brønn eller en artesisk brønn, der mettet kalsium og magnesium grunnvann. I tillegg, sammen med hardhetssalter, kan andre skadelige stoffer også komme dit. Til dette er det nok med kraftig regn og en søppelplass som ligger i distriktet.
Hvor lett det er å forstå mykgjøring av vann - dette er en reduksjon i konsentrasjonen av hardhetssalter i den. Den enkleste versjonen av denne prosessen er termisk (det er også enkel koking). Som nevnt ovenfor, i denne prosessen dekomponerer kalsiumbikarbonat til uoppløselig kalsiumkarbonat, som utfelles, og karbondioksid. Konsentrasjonen av kalsiumsulfat synker også noe. Denne metoden regnes som den enkleste, men ytelsen etterlater mye å være ønsket. Det er også en kjemisk metode, når reagenser tilsettes vann som gjør løselige forbindelser til uløselige. Den største ulempen er at du fortsatt ikke kan drikke en slik væske. Andre metoder krever spesialutstyr.
Utstyr for mykgjøring av vann
I tillegg til plakett på varmeelementene til husholdningsapparater og flekker på vasket lin, er et tegn på hardt vann dårlig skummende såper og pulver, kjøtt som er hardt selv etter lang koking, fraværet av den vanlige aromaen av te og kaffe, som samt den bitre smaken av selve vannet. I tillegg kan vannets hardhet bestemmes ved hjelp av spesielle teststrimler eller en TDS-måler som måler den elektriske ledningsevnen til en væske. Men før du kjøper et filter for mykgjøring av vann, anbefales det å sende det til et laboratorium for analyse, slik at eksperter kan gjøre den mest nøyaktige "diagnosen". For eksempel vil et strømningsfilter for vannmykning bare være relevant for væsker uten et kritisk jerninnhold, og i alvorlige tilfeller er det bedre å bruke en hoved.
Hvilke installasjoner brukes til vannmykning? Eksperter skiller følgende kategorier av filtre:
- Membran. Eliminer opptil 98 % av urenheter, noe som gjør vannet faktisk destillert. Men for at kvaliteten på arbeidet deres ikke skal synke, er det nødvendig å opprettholde et trykk på minst 3–4 atmosfærer i vannforsyningssystemet. En slik enhet er ganske dyr, men den har også lang levetid.
- Polyfosfat. De er en kolbe med krystaller av polyfosfatsalt. Vannet som passerer gjennom dem er mettet med natriumpolyfosfat. Vanligvis festet foran husholdningsutstyr. Polyfosfatfiltre er rimelige, men de må skiftes hver sjette måned. Det anbefales ikke å drikke myknet vann med deres hjelp.
- Magnetisk. Takket være dem virker et konstant magnetfelt på vannet, noe som endrer strukturen til hardhetssalter. Molekylene slutter å kombinere når de varmes opp og danner ikke et bunnfall, og ødelegger også den allerede eksisterende skalaen. Saltkonsentrasjonen forblir den samme, så slike enheter er hovedsakelig egnet for rør og pumpeutstyr. Avhengig av sorten kan magnetfiltre fungere fra 5 til 25 år uten behov for vedlikehold.
- Elektromagnetisk. De fungerer på grunnlag av stråling av elektromagnetiske bølger med den nødvendige frekvensen. De krever en nettverkstilkobling, men bruker ikke mye energi. Kompatibel med alle andre vannmykningssystemer. Overskytende salter blir deretter fjernet gjennom sumpen og inn i kloakken. I tillegg til magnetiske ødelegger de i tillegg skala, men de koster en størrelsesorden dyrere.
- Ionebytterfiltre for mykning av vann. Deres klare pluss er den høye ytelsen og holdbarheten til filterelementet. De er et søyle- eller kabinettfilter, inne i hvilket det er en ionebytterharpiks. Som med magnetfiltre kan kun kaldt vann rengjøres med dem. Filtreringsprosessen består i å erstatte kalsium- og magnesiumioner med natriumioner, som ikke skader menneskekroppen og husholdningsapparater.
Til tross for at etter at ionebyttemetoden for mykning av vann kan drikkes, regnes det som reagens, resten er klassifisert som ikke-reagens.
Å avstryke betyr ikke å mykne
Begrepet "hardt vann" er ikke synonymt med "jernvann". Ferskvann inneholder også jern, som kommer inn i brønner og brønner fra kollapsende bergarter, og inn i rør fra aldrende og korroderte vannrør av jern og stål. Det er ikke vanskelig å bestemme vann overmettet med jern etter øye - det har en karakteristisk metallisk lukt og en gulaktig-turbid fargetone. Med slike indikatorer blir hvite ting også gulaktige etter vask, og brune flekker vises på rørleggerarbeid.
I vårt land bør den tillatte mengden jern i vann ikke overstige 0,3 mg-eq / l. Det anbefalte totale jerninntaket for en voksen er 25 milligram per dag.
"Overdose" kan føre til urolithiasis, tarmlidelser, galleblæresykdommer og tannproblemer, samt dermatitt og utvikling av allergier. Derfor er det ingen vits i å kjøpe vannmyknere, mens man ser bort fra utstyr for fjerning av jern. Det er også annerledes, både kjemisk, når jern ødelegges av reagenser, og mekanisk, når jern dekomponeres ved hjelp av lufting, koagulering og ionebyttemetoden beskrevet ovenfor. Dessuten er det "to i ett" installasjoner som samtidig jobber med vannmykning og fjerning av jern. De sparer plass i huset, eierens budsjett og tiden hans i like stor grad.
Teknologien går raskt fremover, og kanskje en dag vil alt vannet på jorden være usedvanlig rent. Men inntil dette skjer, er tilstedeværelsen av et vannfiltreringssystem et presserende behov, fordi menneskers helse er direkte avhengig av det. Samtidig vil du ikke bruke mye penger på ineffektivt utstyr, så valget av et filter for fjerning av jern og mykgjøring av vann bør behandles nøye.
Vannmykning ved dialyse
Magnetisk vannbehandling
Litteratur
Teoretisk grunnlag for vannmykning, klassifisering av metoder
Vannmykning refererer til prosessen med å fjerne hardhetskationer fra den, dvs. kalsium og magnesium. I samsvar med GOST 2874-82 "Drikkevann" bør vannhardheten ikke overstige 7 mg-eq / l. Visse typer produksjon prosessvann stille krav til dens dype oppmykning, dvs. opptil 0,05,0,01 mg-ekv/l. Vanlig brukte vannkilder har en hardhet som oppfyller standardene for husholdnings- og drikkevann, og trenger ikke oppmykning. Vannmykning utføres hovedsakelig under forberedelsen til tekniske formål. Derfor bør hardheten til vann for mating av trommelkjeler ikke overstige 0,005 mg-eq / l. Vannmykning utføres ved metoder: termisk, basert på oppvarming av vann, dets destillasjon eller frysing; reagens, der ionene i vannet Ca ( II ) og mg ( II ) bindes med forskjellige reagenser til praktisk talt uløselige forbindelser; ionebytte, basert på filtrering av myknet vann gjennom spesielle materialer som utveksler ionene inkludert i sammensetningen deres Na ( I) eller H (1) til Ca (II) ioner og mg ( II ) inneholdt i dialysevannet; kombinert, som representerer ulike kombinasjoner av metodene ovenfor.
Valget av mykgjøringsmetoden bestemmes av dens kvalitet, den nødvendige mykningsdybden og tekniske og økonomiske hensyn. I samsvar med anbefalingene fra SNiP ved oppmykning av grunnvann bør ionebyttemetoder brukes; ved bløtgjøring av overflatevann, når vannavklaring også er nødvendig, brukes kalk- eller kalk-soda-metoden, og når vannet er dypt myknet, påfølgende kationisering. De viktigste egenskapene og betingelsene for bruk av vannmykningsmetoder er gitt i tabell. 20.1.
mykgjørende vann dialyse termisk
For å skaffe vann til husholdnings- og drikkebehov blir vanligvis bare en viss del av det myknet, etterfulgt av blanding med kildevannet, mens mengden myknet vann Q y bestemt av formelen
hvor J o. og. - total hardhet av kildevannet, mg-eq/l; F 0. s. - total hardhet av vann som kommer inn i nettverket, mg-eq / l; J 0. y. - myknet vannhardhet, mg-eq/l.
Vannmykningsmetoder
| Indikator | termisk | reagens | Ionbytte | dialyse |
| Prosesskarakteristikk | Vann varmes opp til en temperatur over 100 ° C, mens karbonat- og ikke-karbonathardhet fjernes (i form av kalsiumkarbonat, hydroksid og magnesium og gips) | Til vannet tilsettes kalk, som eliminerer karbonat- og magnesiumhardhet, samt brus, som eliminerer ikke-karbonat - andre hardhet. | Myknet vann føres gjennom kationittfiltre | Råvann filtreres gjennom en semipermeabel membran |
| Hensikten med metoden | Eliminering av karbonathardhet fra vann som brukes til mating av lav- og middeltrykkskjeler | Grunn mykgjøring med samtidig klaring av vann fra suspenderte faste stoffer | Dyp oppmykning av vann som inneholder en liten mengde suspendert faststoff | Mykgjøring på dypt vann |
| Vannforbruk til eget behov | - | Ikke mer enn 10 % | Opptil 30 % eller mer i forhold til hardheten til kildevannet | 10 |
| Forutsetninger for effektiv bruk: turbiditet av kildevann, mg/l | Opp til 50 | Opp til 500 | Ikke mer enn 8 | Opp til 2.0 |
| Vannhardhet, mg-ekv/l | Karbonathardhet med en overvekt av Ca (HC03) 2, ikke-karbonathardhet i form av gips | 5.30 | Ikke høyere enn 15 | Opp til 10,0 |
| Resthardhet på vann, mg-eq/l | Karbonathardhet opp til 0,035, CaS04 opp til 0,70 | Opp til 0,70 | 0.03.0.05 prn for ett-trinns og opptil 0,01 for totrinns kationisering | 0,01 og under |
| Vanntemperatur, ° С | Opp til 270 | Opp til 90 | Opptil 30 (glaukonitt), opptil 60 (sulfonert kull) | Opp til 60 |
Termisk metode for vannmykning
Det anbefales å bruke den termiske metoden for vannmykning når du bruker karbonatvann som brukes til å mate kjeler. lavtrykk, så vel som i kombinasjon med reagensmetoder for vannmykning. Den er basert på forskyvningen av karbondioksid-likevekten når den varmes opp mot dannelsen av kalsiumkarbonat, som er beskrevet av reaksjonen
Ca (HC0 3) 2 -\u003e CaCO 3 + C0 2 + H 2 0.
Likevekten forskyves av en reduksjon i løseligheten av karbonmonoksid (IV), forårsaket av en økning i temperatur og trykk. Koking kan fullstendig fjerne karbonmonoksid (IV) og dermed redusere kalsiumkarbonat-hardheten betydelig. Imidlertid kan denne hardheten ikke elimineres fullstendig, siden kalsiumkarbonat, selv om det er litt (13 mg / l ved en temperatur på 18 ° C), fortsatt er løselig i vann.
I nærvær av magnesiumbikarbonat i vann skjer prosessen med utfelling som følger: først dannes et relativt godt løselig (110 mg / l ved en temperatur på 18 ° C) magnesiumkarbonat
Mg (HCO 3) → MgCO 3 + C0 2 + H 2 0,
som hydrolyseres under langvarig koking, som et resultat av at et bunnfall av lett løselige bunnfall (8,4 mg / l). magnesiumhydroksid
MgCO3 + H20 → Mg (OH)2 + CO2.
Følgelig, når vann kokes, reduseres hardheten på grunn av kalsium- og magnesiumbikarbonater. Kokende vann reduserer også hardheten bestemt av kalsiumsulfat, hvis løselighet faller til 0,65 g/l.
På fig. 1 viser en termisk mykner designet av Kopiev, som utmerker seg ved anordningens relative enkelhet og pålitelige drift. Det behandlede vannet, forvarmet i apparatet, kommer inn gjennom ejektoren til utløpet av filmvarmeren og sprayes over vertikalt plasserte rør, og strømmer ned gjennom dem mot den varme dampen. Deretter, sammen med avblåsningsvannet fra kjelene, kommer det inn i klaringsanlegget med suspendert sediment gjennom det sentrale tilførselsrøret gjennom den perforerte bunnen.
Karbondioksid og oksygen som frigjøres fra vannet, sammen med overflødig damp, slippes ut i atmosfæren. Kalsium- og magnesiumsaltene som dannes under oppvarming av vann, holdes tilbake i det suspenderte laget. Etter å ha passert gjennom det suspenderte laget, kommer det myknede vannet inn i oppsamleren og slippes ut utenfor apparatet.
Oppholdstiden for vannet i den termiske mykneren er 30,45 min, hastigheten på dens oppadgående bevegelse i det suspenderte laget er 7,10 m/t, og i åpningene til den falske bunnen 0,1,0,25 m/s.

Ris. 1. Termisk mykner designet av Kopiev.
15 - utslipp av dreneringsvann; 12 - sentralt tilførselsrør; 13 - falske perforerte bunner; 11 - suspendert lag; 14 - slamutslipp; 9 - oppsamling av myknet vann; 1, 10 2 - rensing av kjeler; 3 - ejektor; 4 - fordampning; 5 - film varmeapparat; 6 - damputslipp; 7 - en ringformet perforert rørledning for vanndrenering til ejektoren; 8 - skrånende skillevegger
Reagensmetoder for vannmykning
Vannmykning med reagensmetoder er basert på behandling med reagenser som danner tungtløselige forbindelser med kalsium og magnesium: Mg (OH) 2, CaCO 3, Ca 3 (P0 4) 2, Mg 3 (P0 4) 2 og andre, etterfulgt ved at de separeres i klaringsapparater , tynnsjiktsbeholdere og klaringsfiltre. Kalk, soda, natrium- og bariumhydroksider og andre stoffer brukes som reagenser.
Vannmykning ved kalking brukes for sin høye karbonat- og lave ikke-karbonat-hardhet, samt i tilfellet når det ikke er nødvendig å fjerne salter av ikke-karbonat-hardhet fra vann. Kalk brukes som reagens, som introduseres i form av en løsning eller suspensjon (melk) i forvarmet behandlet vann. Oppløsende, kalk beriker vann med OH - og Ca 2+ ioner, noe som fører til binding av fritt karbonmonoksid (IV) oppløst i vann med dannelse av karbonationer og overgang av hydrokarbonationer til karbonat:
CO 2 + 20H - → CO 3 + H 2 0, HCO 3 - + OH - → CO 3 - + H 2 O.
En økning i konsentrasjonen av CO 3 2 - ioner i det behandlede vannet og tilstedeværelsen av Ca 2+ ioner i det, tatt i betraktning de som er introdusert med kalk, fører til en økning i løselighetsproduktet og utfelling av dårlig løselig kalsiumkarbonat:
Ca 2+ + C0 3 - → CaC0 3.
Med et overskudd av kalk utfelles også magnesiumhydroksid.
Mg 2+ + 20Н - → Mg (OH) 2
For å akselerere fjerningen av spredte og kolloidale urenheter og redusere alkaliteten til vannet, brukes koagulering av disse urenhetene med jern(II)sulfat samtidig med kalking. FeS0 4 * 7 H 2 0. Resthardheten til myknet vann under avkarbonisering kan oppnås med 0.4.0.8 mg-eq / l mer enn ikke-karbonat-hardhet, og alkaliteten er 0.8.1.2 mg-eq / l. Kalkdosen bestemmes av forholdet mellom konsentrasjonen av kalsiumioner i vann og karbonathardhet: a) ved forholdet [Ca 2+ ] /20<Ж к,
b) med forholdet [Ca 2+] / 20 > W til,
hvor [СО 2 ] er konsentrasjonen av fritt karbonmonoksid (IV) i vann, mg/l; [Ca 2+ ] - konsentrasjon av kalsiumioner, mg/l; Zhk - karbonathardhet av vann, mg-eq / l; D til - dose koagulant (FeS0 4 eller FeCl 3 når det gjelder vannfrie produkter), mg / l; e til- ekvivalent masse av det aktive stoffet i koaguleringsmidlet, mg/mg-eq (for FeSO 4 e k = 76, for FeCl3 ek = 54); 0,5 og 0,3 - et overskudd av kalk for å sikre en større fullstendighet av reaksjonen, mg-eq / l.
Uttrykket D til /e til tas med et minustegn hvis koagulanten introduseres før kalk, og med et plusstegn hvis sammen eller etter.
I fravær av eksperimentelle data, er dosen av koagulanten funnet fra uttrykket
D c \u003d 3 (C) 1/3, (20.4)
hvor C er mengden suspensjon som dannes under vannmykning (uttrykt i tørrstoff), mg/l.
I sin tur bestemmes C ved hjelp av avhengigheten
hvor M og - innholdet av suspendert stoff i kildevann, mg/l; m- CaO-innhold i kommersiell kalk, %.
Lime-soda-vannmykningsmetode beskrevet av følgende hovedreaksjoner:

I henhold til denne metoden kan gjenværende hardhet økes til 0,5,1, og alkaliniteten fra 7 til 0,8,1,2 mekv/l.
Doser av kalk D og og soda D s (uttrykt i Na 2 C0 3), mg / l, bestemmes av formlene
![]() (20.7)
(20.7)
hvor er innholdet av magnesium i vann, mg/l; Zh n. k. - ikke-karbonat hardhet av vann, mg-eq / l.
Med kalk-soda-metoden for vannmykning, kan det dannede kalsiumkarbonatet og magnesiumhydroksidet overmette løsningene og forbli i en kolloidal-dispergert tilstand i lang tid. Overgangen deres til grovt slam tar lang tid, spesielt ved lave temperaturer og tilstedeværelsen av organiske urenheter i vannet, som fungerer som beskyttende kolloider. Med et stort antall av dem kan vannets hardhet med reagensvannmykning reduseres med bare 15,20 %. I slike tilfeller, før eller under mykning, fjernes organiske urenheter fra vannet med oksidasjonsmidler og koagulanter. Med kalk-soda-metoden utføres prosessen ofte i to trinn. Til å begynne med fjernes organiske urenheter og en betydelig del av karbonathardheten fra vannet, ved å bruke salter av aluminium eller jern med kalk, utfører prosessen under optimale koagulasjonsforhold. Etter det introduseres brus og resten av limen og vannet mykgjøres. Ved fjerning av organiske urenheter samtidig med vannmykning brukes kun jernsalter som koaguleringsmidler, siden ved en høy pH-verdi av vann som er nødvendig for å fjerne magnesiumhardhet, danner aluminiumsalter ikke sorpsjonsaktivt hydroksyd. Dosen av koagulant i fravær av eksperimentelle data beregnes med formelen (20.4). Mengden suspensjon bestemmes av formelen
hvor W o er den totale hardheten til vann, mg-eq / l.
Dypere mykning av vann kan oppnås ved å varme det opp, tilsette et overskudd av et utfellingsmiddel og skape kontakt av det myknede vannet med tidligere dannet nedbør. Når vann varmes opp, reduseres løseligheten av CaCO 3 og Mg (OH) 2 og mykningsreaksjonene fortsetter mer fullstendig.
Fra grafen (fig. 2, a) kan man se at resthardheten, nær det teoretisk mulige, kun kan oppnås ved betydelig oppvarming av vannet. En betydelig mykgjørende effekt observeres ved 35,40°C, ytterligere oppvarming er mindre effektiv. Dypmykning utføres ved temperaturer over 100 ° C. Det anbefales ikke å tilsette et stort overskudd av et utfellingsmiddel under avkarbonisering, siden gjenværende hardhet øker på grunn av ureagert kalk eller hvis det er magnesium ikke-karbonat-hardhet i vannet på grunn av dets overgang til kalsiumhardhet:
MgS0 4 + Ca (OH) 2 \u003d Mg (OH) 2 + CaS0 4

Ris. Fig. 2. Effekt av temperatur (a) og dose av kalk (b) på dybden av vannmykning ved kalk-soda- og kalkmetodene
Ca (0H) 2 + Na 2 C0 3 \u003d CaC0 3 + 2 NaOH,
men et overskudd av kalk fører til en ineffektiv sløsing med brus, en økning i kostnadene for vannmykning og en økning i hydratisert alkalitet. Derfor tas et overskudd av brus ca 1 mg-eq / l. Vannets hardhet som følge av kontakt med det tidligere utfelte sedimentet avtar med 0,3-0,5 mg-eq/l sammenlignet med prosessen uten kontakt med sedimentet.
Kontrollen av vannmykningsprosessen bør utføres ved å justere pH i det mykede vannet. Når dette ikke er mulig, kontrolleres det av verdien av hydratisert alkalitet, som holdes innenfor 0.1.0.2 mekv/l under avkarbonisering, og 0.3.0.5 mekv/l under kalk-soda-mykning.
Med soda-natrium-metoden for å myke vann, behandles det med brus og natriumhydroksid:

På grunn av det faktum at brus dannes ved reaksjonen av natriumhydroksid med bikarbonat, reduseres dosen som kreves for å legge til vann betydelig. Med en høy konsentrasjon av bikarbonater i vann og lav ikke-karbonathardhet, kan overflødig brus forbli i myknet vann. Derfor brukes denne metoden kun under hensyntagen til forholdet mellom karbonat- og ikke-karbonathardhet.
Soda-natrium metode vanligvis brukt til å myke opp vann, hvis karbonathardhet er litt høyere enn ikke-karbonat. Hvis karbonathardheten er omtrent lik ikke-karbonat, kan soda utelates helt, siden den nødvendige mengden for å myke opp slikt vann dannes som et resultat av samspillet mellom bikarbonater og kaustisk soda. Dosen av soda øker ettersom vannets hardhet uten karbonat øker.
Den regenererende brusregenereringsmetoden, basert på fornyelse av brus under mykningsprosessen, brukes i tilberedning av vann for å mate lavtrykksdampkjeler
Ca (HC0 3) 2 + Na 2 C0 3 \u003d CaC0 3 + 2NaHC0 3.
Natriumbikarbonat, som kommer inn i kjelen med myknet vann, brytes ned under påvirkning av høy temperatur
2NaHC0 3 \u003d Na 2 C0 3 + H 2 0 + C0 2.
Den resulterende brusen, sammen med overskuddet, først innført i vannmykneren, hydrolyseres umiddelbart i kjelen med dannelse av natriumhydroksid og karbonmonoksid (IV), som kommer inn i vannmykneren med skyllevann, hvor det brukes til å fjerne kalsium og magnesiumbikarbonater fra det myknede vannet. Ulempen med denne metoden er at dannelsen av en betydelig mengde CO 2 under mykningsprosessen forårsaker korrosjon av metallet og en økning i den tørre rest i kjelevannet.
Barium-vannmykningsmetode brukes i kombinasjon med andre metoder. Først innføres bariumholdige reagenser i vann (Ba (OH) 2, BaCO 3, BaA1 2 0 4) for å eliminere sulfathardhet, deretter behandles det etter klaring av vannet med kalk og soda for ytterligere mykning. Kjemien til prosessen er beskrevet av reaksjonene:

På grunn av de høye kostnadene for reagenser, brukes bariummetoden sjelden. På grunn av toksisiteten til bariumreagenser er det uegnet for tilberedning av drikkevann. Det resulterende bariumsulfatet utfelles veldig sakte, så store sedimenteringstanker eller klaringsmidler er nødvendig. For å introdusere BaCO3 bør det brukes flokkulatorer med mekaniske omrørere, siden BaCO 3 danner en tung, raskt avsetningssuspensjon.
De nødvendige doser av bariumsalter, mg/l, kan finnes ved å bruke uttrykkene: bariumhydroksid (et produkt med 100 % aktivitet) D b =1,8 (SO 4 2-), bariumaluminat D b =128W 0 ; bariumkarbonat D i \u003d 2,07γ (S0 4 2-);
Bariumkarbonat brukes med kalk. Ved påvirkning av karbondioksid på bariumkarbonat oppnås bariumbikarbonat, som doseres i det myknede vannet. I dette tilfellet bestemmes dosen av karbondioksid, mg/l, ut fra uttrykket: D ang. = 0,46 (S042-); hvor (SO 4 2-) er innholdet av sulfater i det myknede vannet, mg/l; γ=1.15.1.20 - koeffisient tatt i betraktning tap av bariumkarbonat.
Oxalate vannmykningsmetode basert på bruken av natriumoksalat og på den lave vannløseligheten til det resulterende kalsiumoksalatet (6,8 mg/l ved 18°C)
Metoden er preget av enkelhet i teknologisk og instrumentell design, men på grunn av de høye kostnadene for reagenset, brukes den til å myke opp små mengder vann.
Fosfatering brukes til å myke opp vann. Etter reagensmykning med kalk-soda-metoden er tilstedeværelsen av gjenværende hardhet (ca. 2 mg-eq/l) uunngåelig, som kan reduseres til 0,02-0,03 mg-eq/l ved ytterligere fosfatmykning. En slik dyp etterbehandling gjør det i noen tilfeller mulig å ikke ty til kationisk vannmykning.
Fosfatering oppnår også større vannstabilitet, reduserer dens korrosive effekt på metallrørledninger og forhindrer karbonatavleiringer på den indre overflaten av rørveggene.
Som fosfatreagenser brukes heksametafosfat, tripolyfosfat (ortofosfat) natrium, etc..
Fosfatmetoden for vannmykning ved bruk av tri-natriumfosfat er den mest effektive reagensmetoden. Kjemien til prosessen med vannmykning med trinatriumfosfat er beskrevet av reaksjonene
Som man kan se fra reaksjonene ovenfor, ligger essensen av metoden i dannelsen av kalsium- og magnesiumsalter av fosforsyre, som har lav løselighet i vann og derfor utfelles ganske fullstendig.
Fosfatmykning utføres vanligvis ved å varme opp vann til 105.150 ° C, og nå mykningen til 0.02.0.03 mg-eq / l. På grunn av de høye kostnadene for trinatriumfosfat, brukes fosfatmetoden vanligvis for å myke opp vann som tidligere er myknet med kalk og brus. Dosen av vannfritt trinatriumfosfat (Df; mg/l) for ytterligere mykning kan bestemmes fra uttrykket
D F \u003d 54,67 (W OST + 0,18),
hvor F ost - gjenværende hardhet av myknet vann før fosfatmykning, mg-eq / l.
Ca 3 (P0 4) 2 og Mg 3 (P0 4) 2 utfellinger dannet under fosfatmykning adsorberer organiske kolloider og kiselsyre godt fra myknet vann, noe som gjør det mulig å avdekke muligheten for å bruke denne metoden for tilberedning av matevann for medium og høytrykkskjeler (58 .8.98.0 MPa).
En løsning for dosering av heksametafosfat eller natriumortofosfat med en konsentrasjon på 0,5-3% tilberedes i tanker, hvor antallet skal være minst to. Innvendige overflater veggene og bunnen av tankene skal dekkes med et korrosjonsbestandig materiale. Tilberedningstid for en 3 % løsning er 3 timer med obligatorisk omrøring med røreverk eller bobler (ved hjelp av trykkluft) måte.
Teknologiske ordninger og strukturelle elementer i kjemiske vannmykningsanlegg
I teknologien for mykning av reagensvann brukes utstyr for tilberedning og dosering av reagenser, blandere, tynnsjikts sedimentasjonstanker eller klaringsapparater, filtre og installasjoner for stabilisering av vannbehandling. Diagrammet av en trykkvannmykner er vist i fig. 3

Ris. 3. Vannmykner med virvelreaktor.
1 - trakt med kontaktmasse; 2 - ejektor; 3, 8 - tilførsel av initial og fjerning av myknet vann; 4 - virvelreaktor; 5 - input av reagenser; 6 - hurtig klaringsfilter; 9 - dumping av kontaktmasse; 7 - myknet vanntank
Det er ikke noe flokkuleringskammer i denne planten fordi kalsiumkarbonatbunnfallet flokkulerer seg i kontaktmassen. Ved behov ryddes vannet foran reaktorene.
Det optimale anlegget for å myke opp vann ved hjelp av kalk- eller kalk-sodametoder er virvelreaktor (trykk eller åpen spirator) ( ris. 20.4). Reaktoren er et armert betong- eller stållegeme, innsnevret nedover (konisk vinkel 5,20°) og fylt til omtrent halve høyden med en kontaktmasse. Hastigheten på vannbevegelsen i den nedre smale delen av virvelreaktoren er 0,8,1 m/s; hastigheten på den oppadgående strømmen i den øvre delen på nivå med dreneringsanordningene er 4,6 mm/s. Som kontaktmasse brukes sand eller marmorflis med en kornstørrelse på 0,2-0,3 mm med en hastighet på 10 kg per 1 m3 av reaktorvolumet. Med en spiralformet oppoverstrøm av vann veies kontaktmassen, sandkornene kolliderer med hverandre, og CaCO 3 krystalliserer intensivt på overflaten deres; Gradvis blir sandkornene til kuler med riktig form. Den hydrauliske motstanden til kontaktmassen er 0,3 m per 1 m høyde. Når diameteren på kulene øker til 1,5,2 mm, frigjøres den største, tyngste kontaktmassen fra den nedre delen av reaktoren og den friske tilsettes. Vortex-reaktorer beholder ikke magnesiumhydroksidsediment, så de bør brukes sammen med filtre installert bak dem kun i tilfeller hvor mengden magnesiumhydroksidsediment som dannes tilsvarer filtrenes skittkapasitet.
Med en smusskapasitet på sandfiltre lik 1,1,5 kg/m 3 og en 8-timers filtersyklus, er den tillatte mengden magnesiumhydroksid 25,35 g/m 3 (magnesiuminnholdet i kildevannet bør ikke overstige 10,15 g/m 3 3). Det er mulig å bruke virvelreaktorer med høyere innhold av magnesiumhydroksid, men samtidig etter dem er det nødvendig å installere klaringsapparater for å skille magnesiumhydroksid.
Forbruket av fersk kontaktmasse tilsatt ved bruk av en ejektor bestemmes av formelen G = 0,045QЖ, hvor G- mengde tilsatt kontaktmasse, kg/dag; F- vannhardhet fjernet i reaktoren, mg-eq/l; Q - installasjonskapasitet, m 3 / t.

Ris. 4. Vortex-reaktor.
1,8 - tilførsel av initial og fjerning av myknet vann: 5 - prøvetakere; 4 - kontaktmasse; 6 - luftutslipp; 7 - en luke for lasting av kontaktmassen; 3 - inngang av reagenser; 2 - fjerning av brukt kontaktmasse
I teknologiske ordninger for mykning av reagensvann med klaringsmidler, brukes vertikale blandere i stedet for virvelreaktorer (fig. 5). I clarifiers bør en konstant temperatur opprettholdes, unngå svingninger på mer enn 1 ° C, i en time, siden konveksjonsstrømmer, sedimentrøring og fjerning av det oppstår.
En lignende teknologi brukes til å myke opp gjørmete vann som inneholder store mengder magnesiumsalter. I dette tilfellet er blanderne lastet med kontaktmasse. Ved bruk av klaringsmidler designet av E.F. Kurgaev, blandere og flokkuleringskamre er ikke gitt, siden blanding av reagenser med vann og dannelse av sedimentflak forekommer i selve klaringsapparatet.
Betydelig høyde med et lite volum av sedimentfortykkere gjør at de kan brukes til vannmykning uten oppvarming, samt for avsilikonisering av vann med kaustisk magnesit. Fordelingen av kildevannet med dyser forårsaker dens rotasjonsbevegelse i den nedre delen av apparatet, noe som øker stabiliteten til det suspenderte laget med svingninger i temperatur og vanntilførsel. Vann blandet med reagenser passerer gjennom horisontale og vertikale blandeplater og kommer inn i sonen for sorpsjonsseparasjon og regulering av slamstrukturen, noe som oppnås ved å endre betingelsene for slamprøvetaking langs høyden av det suspenderte laget, og skaper forutsetninger for å oppnå optimal struktur. , som forbedrer effekten av vannmykning og klaring. Klarere er utformet på samme måte som for konvensjonell vannavklaring.
På bekostning av myknet vann opp til 1000 m 3 /døgn kan et vannbehandlingsanlegg av typen "Jet" brukes. Det behandlede vannet med reagensene tilsatt går inn i tynnlagssumpen og deretter til filteret.
En reagensfri elektrokjemisk vannmykningsteknologi er utviklet ved Institutt for gruvedrift i den sibirske grenen til det russiske vitenskapsakademiet. Bruk av fenomenet alkalisering ved anoden og surgjøring ved katoden når en elektrisk likestrøm passerer gjennom vannsystem, kan vannutslippsreaksjonen representeres ved følgende ligning:
2Н 2 0 + 2е 1 → 20Н - + Í 2,
hvor e 1 er et tegn som indikerer evnen til hardhetssalter til å dissosiere til Ca (II) og Mg (II) kationer.
Som et resultat av denne reaksjonen øker konsentrasjonen av hydroksylioner, noe som forårsaker binding av Mg (II) og Ca (II) ioner til uløselige forbindelser. Fra anodekammeret til en membran (membran laget av belte-type stoff) elektrolysator, passerer disse ionene inn i katodekammeret på grunn av potensialforskjellen mellom elektrodene og tilstedeværelsen av et elektrisk felt mellom dem.
På fig. 6 vist teknologisystem installasjoner for vannmykning ved elektrokjemisk metode.
Produksjonsanlegget ble installert i distriktets kjelehus, som ble testet i ca. to måneder. Metoden for elektrokjemisk behandling viste seg å være stabil, ingen sedimentering ble observert i katodekamrene.
Spenningen på tilførselsdekkene var 16 V, totalstrømmen var 1600 A. Installasjonens totale produktivitet var 5 m3/t, vannhastigheten i anodekamrene var 0,31 n-0,42 m/min, i gapet mellom diafragma og katoden 0,12-0,18 m/min.

Ris. 5. Installasjon av kalk-sodavann mykgjøring.1 ,8 - tilførsel av initial og fjerning av myknet vann; 2 - ejektor; 3 - trakt med kontaktmasse; 5 input av reagenser; 6 - klaringsmiddel med et lag av suspendert sediment; 7 - avklaring hurtigfilter; 4 - virvelreaktor

Ris. 6. Opplegg for installasjon av elektrokjemisk vannmykning I - likeretter VACG-3200-18; 2 - diafragma elektrolysator; 3, 4 - analytt og katalytt; 5 - pumpe; 6 - pH-meter; 7 - klaringsmiddel med et lag med suspendert sediment; 8 - avklarende raskt filter; 9 - utslipp til kloakken; 10, 11 - fjerning av myknet og tilførsel av kildevann; 12 - strømningsmåler; 13 - Avtrekksdeksel
Det er fastslått at fra vann med W o = 14,5-16,7 mg-eq/l oppnås en anolytt med en hardhet på 1,1-1,5 mg-eq/l ved pH = 2,5-3 og en katolytt med en hardhet på 0 ,6-1 mg-ekv/l ved pH=10,5-11. Etter blanding av den filtrerte anolytten og katolytten var indikatorene for myknet vann som følger: den totale hardheten W o var 0,8-1,2 mekv/l, pH = 8-8,5. Strømkostnaden utgjorde 3,8 kWh/m 3 .
Kjemiske, røntgendiffraksjons-, IR-spektroskopiske og spektrale analyser har fastslått at bunnfallet hovedsakelig inneholder CaC0 3, Mg (OH) 2 og delvis Fe 2 0 3 *H 2 0. Dette indikerer at bindingen av Mg (II)-ioner skjer etter telling av hydroksylioner under utslipp av vannmolekyler ved katoden.
Elektrokjemisk behandling av vann før det tilføres til kationittfiltre gjør det mulig å øke driftssyklusen betydelig (15-20 ganger).
Termokjemisk metode for vannmykning
Termokjemisk mykgjøring brukes utelukkende til fremstilling av vann til dampkjeler, siden i dette tilfellet er varmen brukt på oppvarming av vann mest rasjonelt brukt. Ved denne metoden utføres vannmykning vanligvis "ved en vanntemperatur over 100 ° C. Mer intensiv mykning av vann når det varmes opp lettes av dannelsen av tunge og store flak av sediment, dens raskeste sedimentering på grunn av en nedgang i viskositeten til vann ved oppvarming, og kalkforbruket reduseres også, siden fritt karbonmonoksid (IV) fjernes ved oppvarming før innføring av reagenser. Den termokjemiske metoden brukes med og uten tilsetning av et koaguleringsmiddel, siden den høye tettheten av bunnfallet eliminerer behovet for at det skal bli tyngre under utfelling.I tillegg til koaguleringsmidlet brukes kalk og brus med tilsetning av fosfater og sjeldnere natriumhydroksid og brus. Bruken av hydroksidnatrium i stedet for kalk forenkler teknologien til noe forberedelse og dosering av reagenset er imidlertid en slik erstatning ikke økonomisk berettiget på grunn av dens høye pris.
For å sikre fjerning av vannhardhet uten karbonat, tilsettes brus i overkant. På fig. 7 viser virkningen av et overskudd av soda på det gjenværende kalsium og den generelle hardheten til vann under dets termokjemiske mykning. Som det fremgår av grafene kan med et overskudd av brus på 0,8 mg-eq/l, kalsiumhardhet reduseres til 0,2, og total hardhet til 0,23 mg/eq-l. Med ytterligere tilsetning av brus reduseres hardheten enda mer. Restinnholdet av magnesium i vann kan reduseres til 0,05,0,1 mg-ekv/l med et overskudd av kalk (hydratisert alkalitet) på 0,1 mg-ekv/l. På fig. 20.8 viser installasjon av termokjemisk vannmykning.
Kalk-dolomitt metode brukes til samtidig mykning og desilikonisering av vann ved en temperatur på 120 ° C. Med denne mykningsmetoden kan alkaliteten til vann behandlet med kalk eller kalk og brus (uten overskudd) reduseres til 0,3 meq / l med en gjenværende kalsiumkonsentrasjon på 1,5 mg -ekv/l og opp til 0,5 mg-ekv/l med en gjenværende kalsiumkonsentrasjon på 0,4 mg-ekv/l. Kildevannet behandles med kalk-dolomittmelk og klares i en trykkklarer. Deretter passerer den gjennom trykkantrasitt- og Na-kationittfiltre i første og andre trinn.
I klaringsanlegg tas høyden på klaringssonen lik 1,5 m, hastigheten på den oppadgående strømmen under kalking er ikke mer enn 2 mm / s. Oppholdstiden for vann i klaringsapparatet er fra 0,75 til 1,5 timer, avhengig av hvilken type forurensning som skal fjernes. Jern(III)-saltkoaguleringsmiddel anbefales tilsatt i mengden 0,4 mg-eq/l.

Ris. 7. Effekt av overflødig brus på gjenværende kalsium (a) og totalt (b) hardheten til vannet under dets termokjemiske mykning

Ris. 8. Installasjon av kalk-sodavannmykning med fosfattilleggsmykning: 1 - utslipp av slam fra lageret 2,3 - oppsamling av myknet vann; 4 - tilførsel av kalk og brus; 5, 11 - tilførsel av initial og fjerning av myknet vann; 6 - dampinngang; 7, 8 - termoreaktor av første og andre trinn; 9 - tilførsel av trinatriumfosfat; 10 - avklaring raskt filter
Høytemperatur vannmykningsmetode brukes til å myke den nesten helt. Termokjemiske vannmyknere er vanligvis mer kompakte. De består av reagensdispensere, tynnsjikts sedimentasjonstankvarmere eller klaringsapparater og filtre. Doser av kalk D og brus D s, mg / l, med termokjemisk vannmykning

hvor C og og C med - henholdsvis innholdet av CaO og Na 2 C0 3 i det tekniske produktet, %.
Vannmykning ved dialyse
Dialyse er en metode for å separere oppløste stoffer som avviker betydelig molekylvekter. Den er basert på forskjellige diffusjonshastigheter av disse stoffene gjennom en semipermeabel membran som skiller konsentrerte og fortynnede løsninger. Under påvirkning av en konsentrasjonsgradient (i henhold til massevirkningsloven) diffunderer oppløste stoffer gjennom membranen med ulik hastighet mot en fortynnet løsning. Løsningsmidlet (vann) diffunderer i motsatt retning, og reduserer transporthastigheten av oppløste stoffer. Dialyse utføres i membranapparater med nitro- og celluloseacetatfilmmembraner. Effektiviteten til en semipermeabel vannmykningsmembran bestemmes av høye verdier selektivitet og permeabilitet, som den må opprettholde i lang driftstid. Membranselektivitet kan uttrykkes som følger:
(F og - F y) / F og (20.11)
hvor W in - konsentrasjonen av den opprinnelige løsningen (hardhet); W og - hardhet av myknet vann.
I praksis brukes ofte saltreduksjonskoeffisienten - innholdet av C og /C arr. Det gjenspeiler mest fullstendig endringer i driften av membranen forbundet med produksjonen eller påvirkningen av eksterne faktorer.
Det finnes flere hypotetiske modeller for virkningen av semipermeable membraner.
Hyperfiltrasjonshypotese antyder eksistensen av porer i en semipermeabel membran som lar assosiasjoner av vannmolekyler og hydratiserte saltioner passere under dialyse. Grunnlaget for den teoretiske utviklingen var posisjonen at vann og salter oppløst i den trenger gjennom en semipermeabel membran ved hjelp av diffusjon og strømmer gjennom porene.
Sorpsjonsmodell permeabilitet er basert på forutsetningen at på overflaten av membranen og i dens porene adsorbert lag bundet vann med redusert løselighet. Membranene vil være semipermeable dersom de, i det minste i overflatelaget, har porer som ikke overstiger to ganger tykkelsen av det bundne væskelaget.
Diffusjonsmodell går ut fra antagelsen om at komponentene i systemet løses opp i membranmaterialet og diffunderer gjennom det. Selektiviteten til membranen forklares av forskjellen i diffusjonskoeffisienten og løseligheten til komponentene i systemet i materialet.
Elektrostatisk teori er som følgende. Når kildevannet beveger seg i kammeret på den ene siden av den selektive (kationbytter) membranen, og saltlaken på den andre, natriumioner i tilfelle når saltlaken er fremstilt fra en løsning bordsalt, migrerer inn i membranen og videre inn i kildevannet, og kalsiumioner i motsatt retning, dvs. fra hardt vann til saltlake. Dermed fjernes kalsiumioner fra kildevannet og erstattes av ikke-utfellende natriumioner. Samtidig oppstår sideprosesser i kamrene som følger med hovedprosessen for dialyse: osmotisk overføring av vann, overføring av ioner med samme navn, elektrolyttdiffusjon. Disse prosessene avhenger av kvaliteten på membranen.
Utvekslingsligningen mellom ionene i kildevannet og ionene i membranen har formen
hvor x, x- andre ioner som finnes i løsningen og i membranen.
Likevektskonstant
![]()
Utvekslingsligningen er kun skrevet for kalsiumionet, men> faktisk er det nødvendig å ta hensyn til summen av kalsium- og magnesiumioner. Likevekten mellom saltlaken og membranen er:

Hvis k1+ k 2, da
![]()
hvor n er en eksponent, avhengig av hvilke ioner som er i løsningen.
Fra det siste uttrykket kan vi konkludere med at dersom likevektsforholdet mellom natriumioner i saltlake og hardt kildevann er for eksempel 10, så vil hardheten i kildevannet være omtrent 100 ganger mindre enn i saltlake. Areal, m 2, membranoverflate
hvor M er mengden stoff som har passert gjennom membranen; ΔС cf - drivkraften til prosessen, dvs. forskjellen i konsentrasjonene av stoffet på begge sider av membranen; K d - masseoverføringskoeffisient, vanligvis bestemt eksperimentelt eller tilnærmet ut fra uttrykket
![]()
β 1 og β 2 - de tilsvarende koeffisientene for overføringshastigheten av et stoff i en konsentrert løsning til membranen og fra den i en fortynnet; b - membrantykkelse; D er diffusjonskoeffisienten til det oppløste stoffet.
Hardhet av myknet vann etter dialyse:

hvor Cd og Cp er konsentrasjonene av salter ved begynnelsen av apparatet, henholdsvis i dialysatet og i saltlake, mg-eq/l; og Qp - ytelsen til apparatet for henholdsvis dialysat og saltvann, m 3 /h; F d og F r - hardhet av dialysat og saltvann ved begynnelsen av apparatet, mg-eq/l; a er en konstant bestemt av egenskapene til membraner og løsninger;; L- lengden på banen til løsningen i dialysat- og saltvannskamrene til apparatet, m; υ d - bevegelseshastigheten til dialysatet i kammeret, m/s.
Eksperimentell verifisering av ligning (20.13) på MCC-kationittmembraner viste god konvergens av resultater. En analyse av formel (20.13) viser at en reduksjon i bevegelseshastigheten til dialysatet i kamrene til apparatet øker mykningseffekten, en reduksjon i hardheten til myknet vann er direkte proporsjonal med konsentrasjonen av saltlake.
Magnetisk vannbehandling
Nylig, i innenlandsk og utenlandsk praksis, har magnetisk vannbehandling blitt brukt med suksess for å bekjempe skaladannelse og belegg. Mekanismen for påvirkningen av et magnetfelt på vann og dens urenheter ikke er endelig belyst, er det en rekke hypoteser om at E.F. Tebenikhin klassifisert i tre grupper: den første, som kombinerer de fleste av hypotesene, relaterer effekten av et magnetfelt på saltioner oppløst i vann. Under påvirkning av et magnetfelt polarisering og deformasjon av ioner oppstår, ledsaget av en reduksjon i deres hydrering, noe som øker sannsynligheten for deres konvergens, og i ultimate utdanning senter for krystallisering; den andre involverer virkningen av et magnetisk felt på de kolloidale urenhetene i vann; den tredje gruppen kombinerer ideer om mulig påvirkning av et magnetfelt på strukturen til vannet. Dette påvirkning, på den ene siden, kan forårsake endringer i aggregeringen av vannmolekyler, på den annen side forstyrre orienteringen av kjernefysiske spinn av hydrogen i molekylene.
Vannbehandling i et magnetfelt er vanlig for å bekjempe kalkdannelse. Essensen av metoden er at når vann krysser magnetisk kraftlinjer Kalkdannere frigjøres ikke på varmeoverflaten, men i vannmassen. De resulterende løse sedimentene (slam) fjernes ved blåsing. Metoden er effektiv til å behandle vann i kalsiumkarbonatklassen, som utgjør omtrent 80% av vannet i alle vannforekomster i vårt land og dekker omtrent 85% av territoriet.
Vannbehandling med magnetfelt har blitt mye brukt for å bekjempe kalkdannelse i kondensatorer. dampturbiner, i lavtrykks- og lavkapasitets dampgeneratorer, i varmenett og varmtvannsforsyningsnett og ulike varmevekslere, hvor bruk av andre vannbehandlingsmetoder ikke er økonomisk gjennomførbart. Sammenlignet med vannmykning er hovedfordelene med dens magnetiske behandling enkelhet, lave kostnader, sikkerhet og nesten ingen driftskostnader.
Magnetisk behandling av naturlig vann (både ferskt og mineralisert) fører til en reduksjon i intensiteten av beleggdannelse på varmeoverflater bare hvis de er overmettet med både kalsiumkarbonat og kalsiumsulfat på tidspunktet for eksponering for et magnetfelt og forutsatt at konsentrasjonen av fritt karbonmonoksid (IV) mindre enn likevektskonsentrasjonen. Antikalkeffekten E bestemmer tilstedeværelsen av jernoksider og andre urenheter i vann:
hvor m n og m m - massen av belegg dannet på varmeoverflaten under koking under samme betingelser av samme mengde vann, henholdsvis ubehandlet og behandlet med et magnetisk felt, g.
Anti-skalaeffekten avhenger av sammensetningen av vannet, styrken til magnetfeltet, hastigheten på vannbevegelsen og varigheten av oppholdet i magnetfeltet og andre faktorer. I praksis brukes magnetiske enheter med permanente stål- eller ferritt-bariummagneter og elektromagneter (fig. 9). Enheter med permanentmagneter er strukturelt enklere og krever ikke strøm fra strømnettet. I enheter med en elektromagnet er trådspoler viklet rundt kjernen (kjernen), og skaper et magnetfelt.
Den magnetiske enheten monteres på rørledningene i vertikal eller horisontal posisjon ved hjelp av adapterhylser. Hastigheten på vannbevegelsen i gapet bør ikke overstige 1 m/s. Prosessen med drift av apparatet kan være ledsaget av forurensning av passasjegapet med mekaniske, hovedsakelig ferromagnetiske urenheter. Derfor må enheter med permanente magneter periodisk demonteres og rengjøres. Jernoksider fjernes fra elektromagnetiske enheter ved å koble dem fra strømnettet.
Resultatene fra studier av MGSU (G.I. Nikoladze, V.B. Vikulina) viste at for vann med en karbonathardhet på 6,7 µg-eq/l, en oksiderbarhet på 5,6 mg02/l og en saltholdighet på 385,420 mg/l, den optimale magnetfeltstyrken var (10.12.8) * 19 4 A / m, som tilsvarer en strømstyrke på 7,8 A.
Opplegget for installasjon for magnetisk behandling av ekstra matevann for oppvarming av dampkjeler er vist i fig. 20.10.
Nylig har enheter med eksterne magnetiseringsspoler blitt utbredt. For magnetisering av store vannmasser er det laget enheter med lag-for-lag-behandling.
I tillegg til å forhindre kalkdannelse, magnetisk behandling , ifølge P.P. Strokach, kan brukes til å intensivere prosessen med koagulering og krystallisering, akselerere oppløsningen av reagenser, øke effektiviteten ved bruk av ionebytterharpikser og forbedre den bakteriedrepende virkningen av desinfeksjonsmidler.

Ris. 9. Elektromagnetisk apparat for avleiring av vannbehandling SKV VTI: 1,8 - tilførsel av initial og fjerning av magnetisert vann; 2 - nett; 3 - arbeidsgap for passasje av magnetisert vann; 4 - foringsrør; 5 - magnetiseringsspole; 6 - kjerne; 7 - ramme; 9 - lokk; 10 - terminaler
Ved utforming av magnetiske vannbehandlingsenheter spesifiseres følgende data: type enhet, dens ytelse, magnetfeltinduksjon i arbeidsgapet eller tilsvarende magnetfeltstyrke, vannhastighet i arbeidsgapet, tid for vann å passere gjennom den aktive sonen av enheten, type og dens spenning for den elektromagnetiske enheten eller magnetiske legering og magnetdimensjoner for permanentmagnetmaskiner.

Ris. 10. Plan for plassering av en magnetisk installasjon for behandling av kjelevann uten forbehandling.
1,8 - kilde og etterfyllingsvann; 2 - elektromagnetiske enheter; 3, 4 - varmeovner I og II trinn; 5 - avlufter; 6 - mellomtank; 7 - sminkepumpe
Litteratur
1. Alekseev L.S., Gladkov V.A. Forbedring av kvaliteten på bløtt vann. M.,
2. Stroyizdat, 1994
3. Alferova L.A., Nechaev A.P. lukkede systemer vannforvaltning av industribedrifter, komplekser og regioner. M., 1984.
4. Ayukaev R.I., Meltser V.Z. Produksjon og bruk av filtermaterialer for vannrensing. L., 1985.
5. Veitser Yu.M., Miits D.M. Høymolekylære flokkuleringsmidler i vannrenseprosesser. M., 1984.
6. Egorov A.I. Hydraulikk av trykkrørsystemer i VVS behandlingsfasiliteter. M., 1984.
7. Zhurba M.G. Rensing av vann på granulære filtre. Lvov, 1980.